Natria du(trimetil-silicil)amido
| Natria du(trimetil-silicil)amido | |||

| |||
| Kemia strukturo de la Natria du(trimetil-silicil)amido | |||

| |||
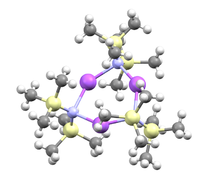
| 3D Kemia strukturo de la Natria du(trimetil-silicil)amido | |||
| |||
| 3D Kemia strukturo de natria du(trimetil-silicil)amido | |||
| Kemia formulo | |||
| CAS-numero-kodo | 1070-89-9 | ||
| ChemSpider kodo | |||
| PubChem-kodo | 2724254 | ||
| Fizikaj proprecoj | |||
| Aspekto | Bruna solido | ||
| Molmaso | 183.37 g mol−1 | ||
| Smiles
| |||
| Denseco | 0,904 g/cm3 | ||
| Fandopunkto | inter 171 kaj 175 °C (inter 340 kaj 347 ℉; inter 444 kaj 448 K) | ||
| Bolpunkto | 170 °C (338 ℉; 443 K) 2 mmHg | ||
| Ekflama temperaturo | 43 ℉ | ||
| Sekurecaj Indikoj | |||
| Risko | R11 R14 R15 R19 R20 R34 R37 | ||
| Sekureco | S8 S16 S24/25 S33 S36 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj[1] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H314, H335, H351 | ||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P210, P240, P242, P243, P260, P264, P271, P280, P301+330+331, P303+361+353 | ||
(25 °C kaj 100 kPa) | |||
Natria du(trimetil-silicil)amido, du(trimetil-silicil)amido de natrio aŭ C6H18NNaSi2 estas organosilicia kombinaĵo, ankaŭ konata kiel heksametiladusiliciazido, forta bazo uzata en malprotonigaj reakcioj aŭ alkalo-katalizaj sintezoj.
La avantaĝo estas ĝia komerca disponebleco kiel solido kiu estas solvebla ne nur en eteroj, tiel kiel kvarhidrofurano[2] aŭ duetila etero[3], sed ankaŭ en aromataj solvantoj, tiel kiel benzeno kaj tolueno pro la lipofila trimetil-silicila grupo. Natria du(trimetil-silicil)amido estas rapide detruita de la akvo por estigi natrian hidroksidon kaj du(trimetil-silicil)aminon.
Proprecoj
[redakti | redakti fonton]Kvankam la ligilo N-Na estas polara kovalento kiel solido, kiam dissolvita en nepolaraj solvantoj ĉi-komponaĵo estas trimera, konsistanta je centra ringo Na3N3.
Natria du(trimetil-silicil)amido uzatas en organikaj sintezoj ĉefe por:
- Malprotonigi ketonojn kaj esterojn por generi enolatajn[4] derivaĵojn.
- Generi karbenojn (=CH2) per senhalogenidigo de karbono-halogenidoj. Ĉi-reakciantaj karbenoj unuiĝas al alkenoj por doni substituitajn ciklopropanojn kaj ciklopropenojn.
- Malprotonigo de fosfoniaj saloj (PH4+) generante reakcianto de Wittig[5]
- Konverti alkilaj halogenidoj al aminoj en duetapa procezo komencante per n-alkiligo sekvata de hidrolizo de la ligiloj N-Si.
Literaturo
[redakti | redakti fonton]- Sigma Aldrich
- Chemical Book
- Santa Cruz Biotechnology Arkivigite je 2016-03-04 per la retarkivo Wayback Machine
- Organosilicon Heteropolymers and Heterocompounds, S. N. Borisov
- Issues in Chemistry and General Chemical Research: 2011 Edition
- Organosilicon Chemistry: 2: Plenary Lectures Presented at the Second ..., Yong Zhou
| ||||||
Referencoj
[redakti | redakti fonton]- ↑ Gelest
- ↑ Direct Approaches Toward Natural Product Synthesis. Arkivita el la originalo je 2016-03-04. Alirita 2015-10-11.
- ↑ Organosilicon Chemistry: 2: Plenary Lectures Presented at the Second ..., Yong Zhou
- ↑ Enolo estas organika funkcio kie hidroksila grupo (OH) ligiĝas al primara karbono kun duobla ligo.
- ↑ Georg Wittig (1897-1987) estis germana kemiisto.




